类器官研究需求或将增加——FDA不再要求药物上市前进行动物试验
来自:junmin 更新日期:2023/3/15 点击量: 3790
|
图源:《Science》FDA no longer has to require animal testing for new drugs
2023年1月10日,随着美国参议院最新的一项法案签署生效,FDA宣布将不再要求新药上市前必须进行动物试验。这标志着持续了80多年的药物安全监管条例走向历史尽头。
新规的出炉,引起各界广泛关注和讨论。它不仅意味着规则新旧交替,也将为多种非动物试验的技术手段带来前所未有的增长需求。以下,我们回到最初,从最开始为大家捋清这一事件的来龙去脉。 1938年,美国立法规定新药在推出市场前,必须在动物身上进行安全性和有效性的测试实验,而实验结果必须通过FDA认可,并符合药物安全规定后才能获批上市销售。而FDA要求进行的实验动物来源通常为小鼠、大鼠、猴或狗。保守估计,每年有数万只动物参与此类实验,并随后被安排执行安乐死处理。
动物实验早已有之,著名的条件反射理论提出者——巴普洛夫,就曾通过将食物有无和信号灯颜色关联起来,完成了狗-食物-信号灯的关联建立。
图源:可画
动物实验之重要,在于通过动物身上测试的结果,可以预测人类进行此活动的结果,并提示潜在的风险和效果。对于治疗手段,尤其是药物的安全使用,例如服用剂量、毒性控制等,如果能有大量的动物实验数据支持,将大大降低药物用在人身上的风险。
既然如此,为什么这项持续了80多年的法案会在2023年走向终点?原因很多,其中最主要的应该是以下3个方面。 首先,法案的提出和推动来源于团队或组织,这其中最重要的就是人道主义经济组织、动物关怀组织的提出。
其次,是现有动物实验技术的局限性导致,哈佛大学工程师Don Ingber表示,尽管药物在进入人体临床试验前进行了大量的动物实验,但每年仍有90%以上的药物开发,在人体临床试验阶段仍然出现了安全风险和无任何效果的现象,这意味着前面所做的大量动物试验很可能是没有意义的。
最后,就是近十几年来,非动物手段的模拟试验技术越来越多,且逐渐走向成熟,例如生物芯片、结合大数据的软件模拟、有别于常规细胞体外培养的类器官研究技术等,在逐步获得认可。
图源:可画
尽管FDA明确表示,现阶段虽然不再要求企业提供动物试验的数据,但也不会拒绝动物试验的数据。但由新法案带来的短期混乱,和新技术的迭代与需求,对整个行业的发展改变将是一个大趋势。作为药物研发机构和企业,我们更应该关注如何在新规下,利用新技术加速药物开发,确保药物安全性和有效性。
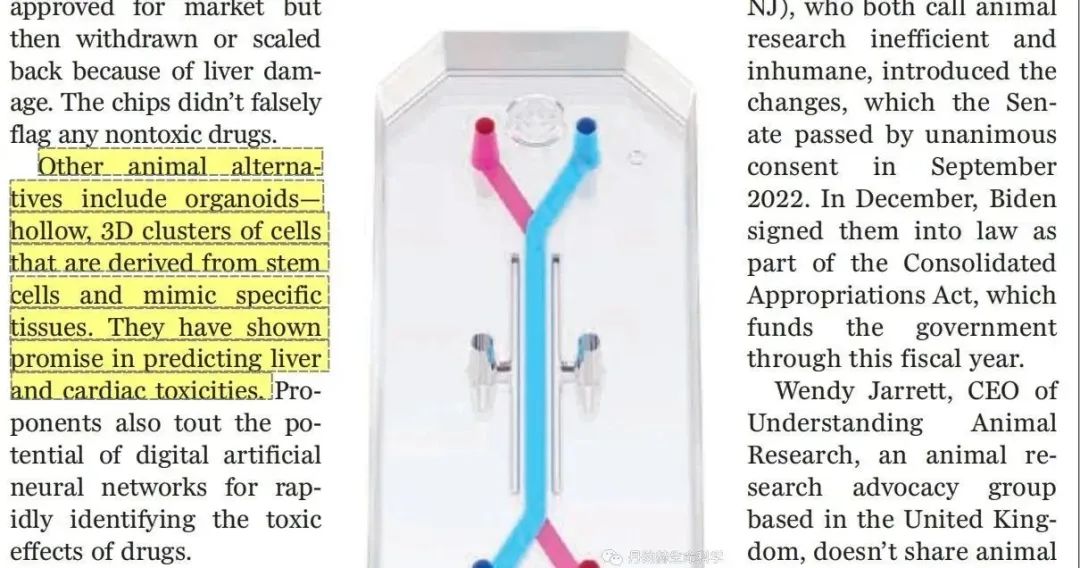
而本文援引的这篇《Science》的报道,还特别提到了在当前新政策环境下, 药物开发者可以把目光放在干细胞来源的类器官技术来代替部分动物试验,因为其在肝、心脏毒性试验中表现出良好的数据结果。
图源:《Science》FDA no longer has to require animal testing for new drugs
类器官——动物试验的另一个替代思路 接下来,我们以类器官技术为例,向您阐述药物开发领域可以利用类器官做什么。
类器官(Organoid)是来源于干细胞或器官组织的细胞,经过体外三维培养,可分化和自组织形成具有宿主相应器官的部分特定功能和结构的细胞团。通俗来说,类器官就是通过体外3D培养技术形成的“类似”器官的生物结构。
类器官这个概念的确立,是源于2009年,荷兰Hans Clevers研究团队证实了体外培养的肠道干细胞能够形成类器官这一研究发现。随后,越来越多科学家们利用多能干细胞和原代成体干细胞培育出多种类器官。
与常规的细胞体外培养技术相比,类器官突破了细胞在体外生长的平面状态,形成了更接近于体内形态的三维结构。这一点,让后者无论从结构还是生理表征上,更趋于“真实”。因此,使用类器官进行基础研究获得的数据,也就更加接近体内的真实情况。
类器官技术为基础研究提供了许多新的实验模型和方法,主要包括以下三个方面: 研究发病机制 类器官模型最显著的优势是人源性和近生理性,肿瘤患者来源的类器官为研究复杂的、尚未阐明的风险基因位点和表型高度异质性的疾病机制提供可能。
药物筛选 在药物研究中,尤其是针对罕见病或缺乏大规模临床试验时,类器官能够为深度测序和功能测试、突变位点或表型分析提供足够资源,是药物毒性预测、新药筛选、个体化治疗的较好模型。
精准治疗 精准医疗的基本理念是整合个性化疾病信息,从而针对每个患者制定精准的诊断和治疗策略。对于癌症精准治疗而言,体外模型必须在生物学特性、基因突变谱上与体内肿瘤保持一致,而且能够维持高度异质性和基因型稳定性,如今肿瘤类器官的出现为癌症精准医疗创造了新的机遇。
近几年,抗癌药物筛选、药物毒性分析、寻找潜在治疗靶点已经成为肿瘤类器官研究的热点领域。此外,随着肿瘤类器官培养技术的优化,已经建立起重建肿瘤微环境的方法,为研究肿瘤微环境与肿瘤细胞的互作提供了一个更成熟的模型。
基于以上信息,在药物开发阶段的动物试验中的某些项目,可以考虑使用类器官来进行替代。比如毒性试验,包括药物的免疫毒性试验,其针对特定脏器的细胞水平毒性上的检测指标,例如T淋巴细胞增殖反应则可以考虑应用分化后的类器官进行检测。无论是使用显微成像观察细胞形态,还是高内涵成像观察组织结构特征的变化,或者是流式细胞术分析细胞表面抗原表位,这些都是有成熟的解决方案。
作为药效评估的测试,例如抗癌药物功效,我们甚至可以畅想,原来必须通过给动物做成瘤实验,然后再进行药物作用评价肿瘤变化的测试,是否可以使用宿主癌细胞分化培养成的类器官进行功效测试?后者不仅能批量培养,检测通量更高,而且肿瘤来自于人体,其各方面的实验指标也会更接近人体疾病的真实情况。
以上,仅是我们对其中一种非动物试验技术的浅显探讨,除了类器官,像大数据模拟的软件分析、生物芯片也是有丰富的应用场景和潜力。作为药物开发者来说, 应尽快把目光转移至此类技术上,并投入精力和资源应对新规。
图源:可画
丹纳赫生命科学的解决方案 丹纳赫生命科学通过对旗下品牌的优质设备资源进行整合,提供针对类器官研究从类器官制备到鉴定,以及后续延申的科研应用的完整解决方案。
1、组织/细胞收集 制备类器官的培养基成分差异将造成细胞的发育与分化的差异。丹纳赫生命科学旗下贝克曼库尔特的Vi-CELL MetaFLEX高速细胞培养生化分析仪,能够快速鉴定培养基组分,具有35s快速检测、系统免维护等优点。
贝克曼库尔特Vi-CELL MetaFLEX高速细胞培养生化分析仪
贝克曼库尔特的Avanti J-15R冷冻离心机采用UHT(Ultra Harmonic Technology)超平稳技术,离心速度稳定准确。同时,搭配加减速脉冲功能,缓慢增减速有效防止高速制动带来的细胞损伤。 
贝克曼库尔特Avanti J-15R冷冻离心机
2、3D培养的换液与用药 贝克曼库尔特自动化工作站Biomek系列,用吸头移液方法实现自动化实验操作,是类器官自动化培养与换液的全能助手。可匹配后续核酸提取以及二代测序DNA/RNA建库流程,实现从细胞培养到分析应用的全自动化。
贝克曼库尔特Biomek i5实验室自动化工作站
对于有药筛实验需求的研究,可在Biomek自动化系统基础上搭配Echo 650移液工作站。利用Echo无接触、体积小的特点,将化合物转移到实验板里。
贝克曼库尔特Echo 650移液工作站
3、类器官检测与鉴定 类器官培养后一般需要进行质控的过程,最常见的手段是检测特异性的细胞表面抗原,从而确定是否发生了明显的细胞分化。另外,细胞凋亡情况、细胞活力也是常见的检测参数。贝克曼库尔特提供CytoFLEX系列流式细胞仪,具有操作简单、高灵敏度等特点。
贝克曼库尔特CytoFLEX系列流式细胞仪
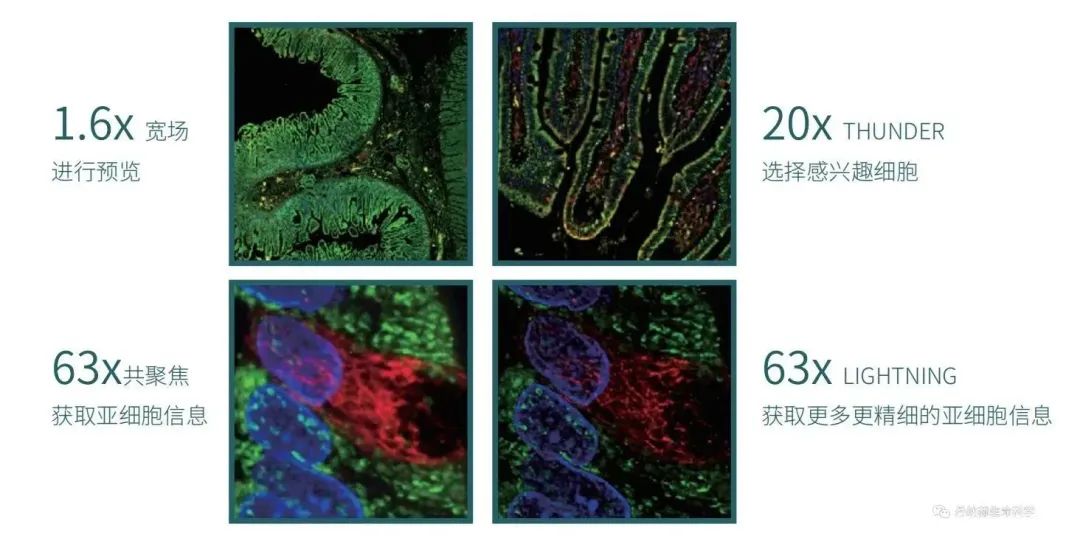
使用一般的倒置显微镜较难清晰观察到类器官的多层组织结构,因此需要利用到共聚焦成像、3D成像等新技术手段。丹纳赫生命科学旗下徕卡显微系统的M系列研究体视镜与荧光体视镜,可以直接多角度、多维度观察细胞的形态与结构。
Leica还提供MICA多模态显像成像系统,满足不同检测精细度及应用目的需要,还可以直接培养并观察细胞。
Leica MICA多模态显像成像系统
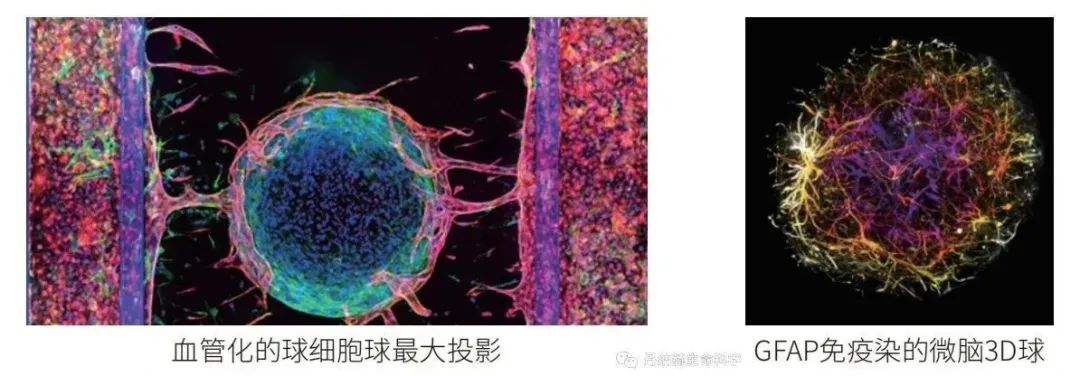
此外,丹纳赫生命科学旗下美谷分子仪器的ImageXpress Confocal HT. ai智能型共聚焦高内涵成像与分析平台,在药效鉴定、药毒性筛查、科学研究中提供各种类型类器官模型高通量成像与3D分析。
MD ImageXpress Confocal HT.ai 智能型共聚焦高内涵成像与分析平台
文章转载来源:丹纳赫生命科学
|